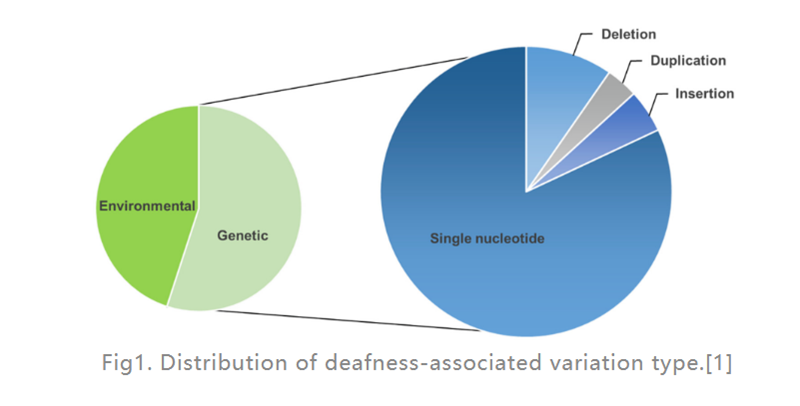
Heyrnarskerðing (HL) er algengasti skynörvandi sjúkdómur hjá mönnum.Í þróuðum löndum eru um 80% tilfella heyrnarleysis fyrir tungu hjá börnum af völdum erfðafræðilegra þátta.Algengast er að gallar séu eins gena (eins og sést á mynd 1), 124 genabreytingar hafa reynst tengdar heyrnarskerðingu án heilkennis í mönnum, restin er af völdum umhverfisþátta.Kuðungsígræðsla (raftæki sett í innra eyrað sem veitir raförvun beint til heyrnartaugarinnar) er lang árangursríkasti kosturinn til að meðhöndla alvarlegt HL, á meðan heyrnartæki (ytra rafeindatæki sem umbreytir og magnar hljóðbylgjur) getur hjálpað sjúklingum með miðlungs HL.Hins vegar eru engin lyf í boði til að meðhöndla arfgengt HL (GHL).Á undanförnum árum hefur genameðferð fengið aukna athygli sem vænleg aðferð til að meðhöndla truflun á innra eyra.
Mynd 1.Dreifing afbrigði sem tengist heyrnarleysi.[1]
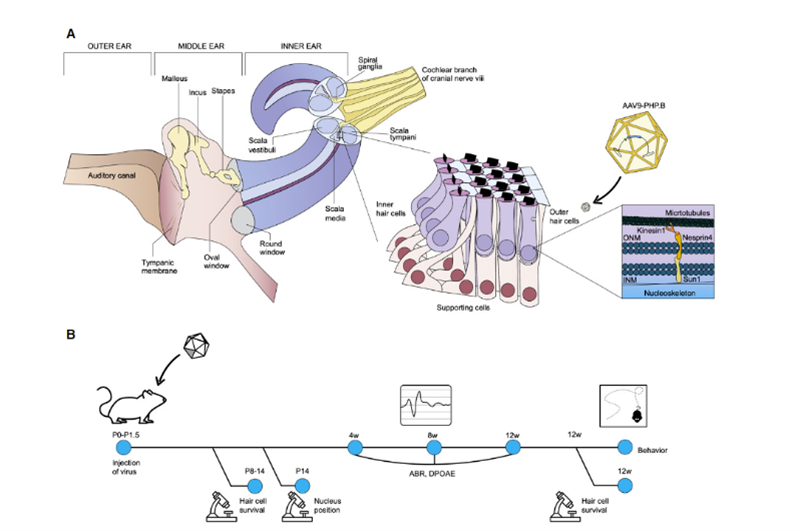
Nýlega birtu vísindamenn frá Salk Institute og University of Sheffield rannsóknarniðurstöðu í Molecular Therapy – Methods & Clinical Development [2], sem sýndi víðtæka notkunarmöguleika fyrir in vivo genameðferð við arfgengri heyrnarleysi.Uri Manor, aðstoðarprófessor við Salk Institute og forstöðumaður Waitt Center for Advanced Biophotonics, sagði að hann fæddist með alvarlega heyrnarskerðingu og fannst að endurheimt heyrnar væri dásamleg gjöf.Fyrri rannsóknir hans komust að því að Eps8 er aktínstýrandi prótein með aktínbindingu og lokunarvirkni;í kuðungshárfrumum er próteinfléttan sem myndast af Eps8 með MYO15A, WHIRLIN, GPSM2 og GNAI3 aðallega til staðar. Til að viðhalda hárknippum, sem ásamt MYO15A staðsetja BAIAP2L2 á oddum styttri stereócilia, er nauðsynlegt til að viðhalda hárknippum.Þess vegna getur Eps8 stjórnað lengd stereocilia hárfrumna, sem er nauðsynlegt fyrir eðlilega heyrnarstarfsemi;Eps8 eyðing eða stökkbreyting mun leiða til stuttra stereocilia, sem gerir það að verkum að það getur ekki umbreytt hljóði almennilega í rafboð fyrir skynjun heilans, sem aftur leiðir til heyrnarleysis..Á sama tíma fann samstarfsmaðurinn Walter Marcotti, prófessor við háskólann í Sheffield, að hárfrumur geta ekki þróast eðlilega ef Eps8 er ekki til.Í þessari rannsókn tóku Manor og Marcotti saman til að kanna hvort að bæta Eps8 við stereociliary frumur gæti endurheimt virkni þeirra og aftur á móti bætt heyrn hjá músum.Rannsóknarteymið notaði adeno-associated virus (AAV) vektor Anc80L65 til að afhenda kóðaröðina sem inniheldur villigerð EPS8 inn í kuðunginn á Eps8-/- nýfæddum P1-P2 músum með hringhimnusprautun;í hárfrumum músa Kuðungshárfrumum Virkni stereócilia var lagfærð áður en þau þroskuðust;og viðgerðaráhrifin einkenndust af myndtækni og mælingum á stereocilia.Niðurstöðurnar sýndu að Eps8 jók lengd stereocilia og endurheimti starfsemi hárfrumna í lágtíðni frumum.Þeir komust einnig að því að með tímanum virtust frumurnar missa getu sína til að bjargast með þessari genameðferð.Merkingin er sú að það gæti þurft að gefa þessa meðferð í móðurkviði, þar sem Eps8-/- hárfrumur gætu hafa þroskast eða safnast upp skemmdum sem ekki er hægt að gera við eftir að mýsnar fæddust."Eps8 er prótein með margar mismunandi aðgerðir, og það er enn mikið að kanna," sagði Manor.Framtíðarrannsóknir munu fela í sér að kanna áhrif Eps8 genameðferðar til að endurheimta heyrn á mismunandi þroskastigum og hvort mögulegt sé að lengja meðferðarmöguleika.Fyrir tilviljun, í nóvember 2020, birti prófessor KarenB Avraham við Tel Aviv háskólann í Ísrael niðurstöður sínar í tímaritinu EMBO Molecular Medicine [3], með því að nota nýstárlega genameðferðartækni til að búa til skaðlausa tilbúna adenó-tengda veiru AAV9-PHP.B, Gengallinn í hárfrumum Syne4-/- músa var lagfærður með því að sprauta veiru sem ber kóðaröð Syne4 inn í innra eyra músa, sem gerir honum kleift að komast inn í hárfrumurnar og losa erfðaefnið sem borið er, sem gerir þeim kleift að þroskast og starfa eðlilega (eins og á mynd 2).
Mynd 2.Skematísk framsetning á líffærafræði innra eyra, með áherslu á líffæri Corti og frumuvirkni nesprin-4.
Það má sjá að notkun genameðferðar til að ná þeim tilgangi að meðhöndla arfgenga sjúkdóma á genastigi með því að setja inn, fjarlægja eða leiðrétta einhver stökkbreytt gen til meðferðar (þ.e. stjórna erfðabreytingum sjúkdómsins) hefur mikil klínísk áhrif.umsóknarhorfur.Núverandi genameðferðaraðferðum fyrir erfðafræðilega skort heyrnarleysi má skipta í eftirfarandi flokka:
genaskipti
Genuppskipti eru að öllum líkindum „einfaldasta“ form genameðferðar, byggt á því að greina og skipta út gölluðu geni fyrir eðlilega eða villigerða afrit af geninu.Fyrsta árangursríka rannsóknin á genameðferð í innra eyra fyrir heyrnarskerðingu af völdum eyðingar á vesicular glutamate transporter 3 (VGLUT3) geninu;AAV1-miðluð sending utanaðkomandi VGLUT3 oftjáningar í hárfrumum í innra eyra (IHCs) getur leitt til viðvarandi endurheimtar heyrnar, bata í taugamótaformi að hluta og krampaviðbragða [4].Hins vegar, í dæmunum, þar á meðal tveimur AAV-afhentum genaskiptum sem lýst er í innganginum hér að ofan, er mikilvægt að hafa í huga að músalíkönin sem notuð eru fyrir ákveðnar gerðir af arfgengum heyrnartapum eru tímabundið frábrugðnar mönnum og hjá P1 músum er innra eyrað á þroskastigi.Hins vegar fæðast menn með þroskað innra eyra.Þessi munur kemur í veg fyrir mögulega notkun músarniðurstaðna við meðhöndlun á arfgengum heyrnarleysissjúkdómum hjá mönnum nema genameðferð berist í þroskuð músaeyru.
Genabreyting: CRISPR/Cas9
Í samanburði við „genaskipti“ hefur þróun genabreytingartækni leitt til dögunar að meðhöndla erfðasjúkdóma frá rótinni.Mikilvægt er að genabreytingaraðferðin bætir upp galla hefðbundinna oftjáningar genameðferðaraðferða sem henta ekki ríkjandi arfgengum heyrnarleysissjúkdómum og þann vanda að oftjáningaraðferðin endist ekki lengi.Eftir að kínverskir vísindamenn slógu út Myo6C442Y stökkbreyttu samsætuna í Myo6WT/C442Y músum með því að nota AAV-SaCas9-KKH-Myo6-g2 genabreytingarkerfið, og innan 5 mánaða frá útsláttinum, voru mýs heyrnarvirkni líkansins endurheimt;á sama tíma sást einnig að lifunartíðni hárfrumna í innra eyra batnaði, lögun cilia varð regluleg og raflífeðlisfræðilegir vísbendingar voru leiðréttar [5].Þetta er fyrsta rannsóknin í heiminum sem notar CRISPR/Cas9 tækni til að meðhöndla arfgenga heyrnarleysi af völdum Myo6 genastökkbreytinga og er hún mikilvæg framfarir í rannsóknum á genabreytingartækni til meðferðar á arfgengum heyrnarleysi.Klínísk þýðing meðferðar veitir traustan vísindalegan grunn.
Afhendingaraðferðir genameðferðar
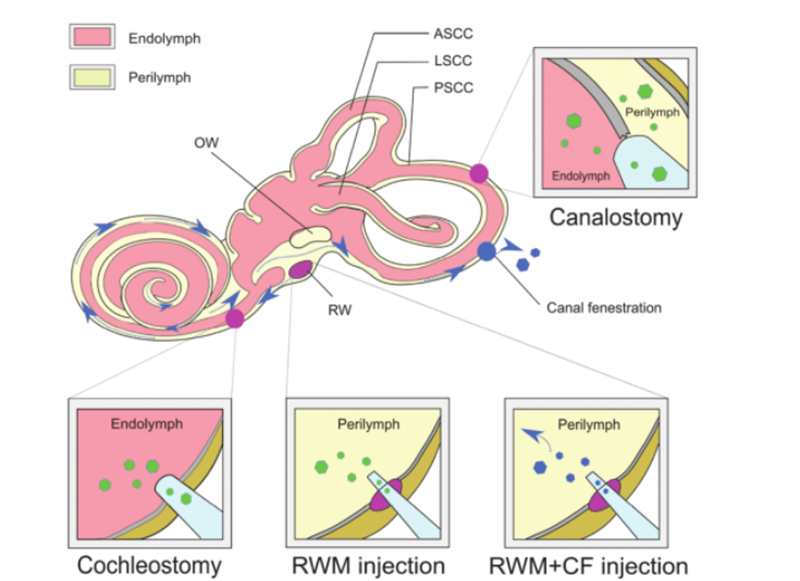
Til að genameðferð skili árangri geta naktar DNA sameindir ekki komist í gegnum frumur á áhrifaríkan hátt vegna vatnssækni þeirra og neikvæðrar hleðslu fosfathópa og til að tryggja heilleika kjarnsýrusameindanna sem bætt er við þarf að velja örugga og áhrifaríka aðferð.Bætt DNA er afhent markfrumunni eða vefnum.AAV er mikið notað sem burðarefni til sjúkdómsmeðferðar vegna mikillar sýkingaráhrifa, lágs ónæmisvaldandi eiginleika og víðtækrar suðrænnar veðra í ýmsar vefjagerðir.Um þessar mundir hefur mikil rannsóknavinna ákvarðað hitabelti mismunandi undirtegunda AAV miðað við mismunandi frumugerðir í músarkuðlinum.Með því að nota AAV afhendingareiginleika ásamt frumusértækum örvum er hægt að ná frumusértækri tjáningu, sem getur dregið úr áhrifum utan miða.Að auki, sem valkostur við hefðbundna AAV vektora, eru stöðugt verið að þróa nýjar tilbúnar AAV ferjur sem sýna yfirburða flutningsgetu í innra eyra, þar af AAV2/Anc80L65 sem er mest notaður.Aðferðir sem ekki eru veirur má skipta frekar í eðlisfræðilegar aðferðir (örsprautun og rafskaut) og efnafræðilegar aðferðir (lípíð-undirstaða, fjölliða-undirstaða og gull nanóagnir).Báðar aðferðirnar hafa verið notaðar við meðferð á arfgengum heyrnarleysissjúkdómum og hafa sýnt mismunandi kosti og takmarkanir.Til viðbótar við afhendingarburðarefnið fyrir genameðferð sem burðarefni, er hægt að beita mismunandi aðferðum við genagjöf in vivo á grundvelli mismunandi markfrumugerða, lyfjagjafarleiða og lækningalegrar virkni.Hin flókna uppbygging innra eyraðs gerir það að verkum að erfitt er að ná til markfrumna og dreifing erfðabreytiefna er hæg.Himnu völundarhúsið er staðsett innan beina völundarhússins í tímabeininu og inniheldur kuðungsrás, hálfhringlaga rás, utricle og blöðru.Hlutfallsleg einangrun þess, lágmarks sogæðablóðrás og aðskilnaður frá blóði með blóð-völundarhússhindrun takmarkar skilvirka altæka afhendingu meðferðarlyfja eingöngu til nýburamúsa.Til að fá veirutítra sem henta fyrir genameðferð er beinni staðbundinni inndælingu veiruferja í innra eyrað nauðsynleg.Stöðugar inndælingarleiðir eru [6]: (1) himna með hringglugga (RWM), (2) barkastóma, (3) heilablóðfalls- eða perilymphatic cochleostomia, (4) himna með hringglugga auk Tube fenestration (CF) (eins og á mynd 3).
Mynd 3.Innra eyra sending genameðferðar.
Þrátt fyrir að margar framfarir hafi orðið í genameðferð, byggðar á klínískum þýðingarmarkmiðum, þarf að vinna meira áður en genameðferð getur orðið fyrsta val meðferðarúrræðis fyrir sjúklinga með erfðasjúkdóma, sérstaklega í þróun öruggra og áhrifaríkra smitferja og fæðingaraðferða.En við trúum því að í náinni framtíð muni þessar tegundir meðferða verða fastur liður í persónulegri meðferð og munu hafa gríðarlega jákvæð áhrif á líf fólks með erfðasjúkdóma og fjölskyldur þeirra.
Foregene hefur einnig hleypt af stokkunum skimunarsetti með miklum afköstum fyrir markgena, sem er hratt og getur framkvæmt öfuga umritun og qPCR viðbrögð án RNA útdráttar.
Vörutenglar
Cell Direct RT-qPCR Kit—Taqman/SYBR GREEN I
Fyrir frekari upplýsingar um vöru, vinsamlegast hafðu samband við:
Pósttími: 02-02-2022